Zahnerhalt am Limit: Palliative Strategien bei verlorenem Parodont
Der Begriff „palliativ” ist in der Medizin fest etabliert, wird in der Zahnmedizin jedoch noch vergleichsweise selten bewusst eingesetzt. Palliative Strategien richten sich an Menschen, bei denen aufgrund psychischer oder körperlicher Einschränkungen, eingeschränkter Belastbarkeit oder begrenzter Lebenserwartung kein umfangreicher Zahnersatz möglich oder sinnvoll ist.
Auch Situationen, in denen geplanter Zahnersatz über längere Zeit hinausgeschoben wird, fallen in die palliative Phase. Ziel ist es nicht, ideale Verhältnisse herzustellen, sondern Beschwerden zu vermeiden, die Kaufunktion zu erhalten und die Lebensqualität zu sichern.
Wann palliative Ansätze sinnvoll sind
Gerade bei fortgeschrittener Parodontitis der Stadien III und IV stellt sich die Frage nach dem Zahnerhalt besonders deutlich. Ausgeprägter Knochenabbau, tiefe Taschen, Zahnwanderungen, Furkationsbefall Grad II und III sowie Zahnlockerungen prägen das klinische Gesamtbild. In palliativen Konzepten wird der Fokus jedoch bewusst verschoben.
Wenn chirurgische oder regenerative Maßnahmen keine ausreichende Stabilisierung erreichen oder aufgrund der individuellen Situation nicht möglich sind, rückt der Zahnerhalt durch nichtchirurgische Maßnahmen in den Vordergrund. Gelingt es dabei, die bakterielle Belastung zu kontrollieren, akute Entzündungen zu vermeiden und Überbelastungen zu reduzieren, können auch stark kompromittierte¹ und gelockerte Zähne über längere Zeit beschwerdefrei im Mund verbleiben.
Okklusionsanpassungen, die Reduktion traumatischer Kontakte und gegebenenfalls Schienungen können dazu beitragen, die Situation zu stabilisieren² und den Patientinnen und Patienten Sicherheit zu vermitteln.
Strategie 1: Mundhygienemaßnahmen genau überprüfen und korrigieren
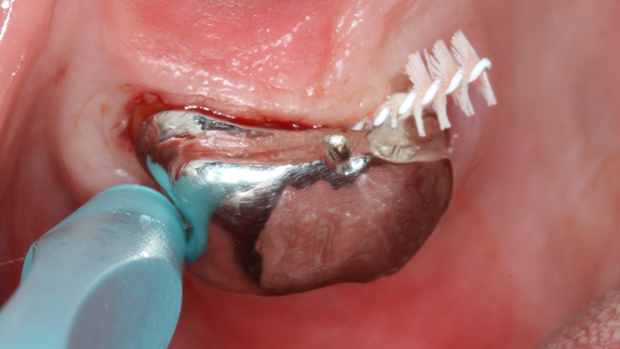
Die Basis jeder palliativen Parodontalstrategie bleibt eine kontinuierlich individuell angepasste Mundhygieneaufklärung.³ Sie muss realistisch, alltagstauglich und auf die vorhandenen Ressourcen abgestimmt sein (Abb. 2). Wenn bereits angewendete Instruktionen nicht greifen, lohnt es sich, die eigene Vorgehensweise zu hinterfragen und neu zu strukturieren.
Dabei solltest du unterschiedliche Lerntypen⁴ berücksichtigen, während der Fokus auf einer klaren Systematik liegt.⁵ Eine aktive Compliance der Patientinnen und Patienten ist nahezu immer entscheidend, um bei zahnärztlichen Therapien die besten Ergebnisse zu erzielen.⁶
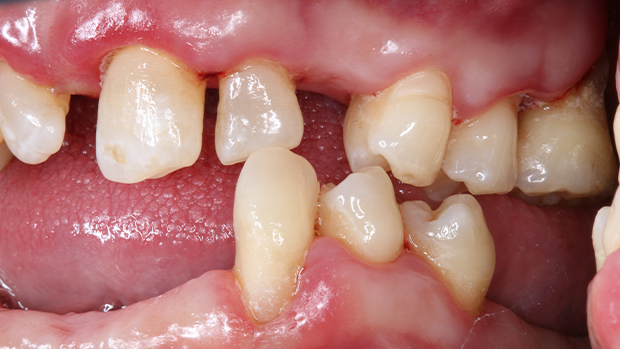
Immer unter der Prämisse, dass keine Beschwerden bestehen, kann bei stark eingeschränkten Patientinnen und Patienten eine reduzierte, gezielt angepasste Mundhygiene nach dem Prinzip „weniger ist mehr” dazu beitragen, die Kaufunktion und damit die allgemeine Gesundheit zu erhalten (Abb. 3).
Strategie 2: Individuelle Risikofaktoren genauer hinterfragen
Gleichzeitig rücken individuelle Risikofaktoren⁷ stärker in den Fokus. Systemische Erkrankungen wie Diabetes⁸, Adipositas⁹ oder Rheuma¹⁰ stehen in einem bidirektionalen Zusammenhang mit Parodontitis. Sie erhöhen das Entzündungsrisiko und werden durch chronische Entzündungen im Mund wiederum negativ beeinflusst. Häufig werden bislang unerkannte Diabetesfälle oder Prädiabetes erstmals durch Veränderungen im Mund sichtbar.
Vorsorge aktiv ansprechen
Deshalb solltest du deine Patientinnen und Patienten regelmäßig auf ärztliche Check-ups hinweisen, insbesondere vor dem Hintergrund, dass laut einer Umfrage nur 37 Prozent der Deutschen regelmäßig Vorsorgeuntersuchungen wahrnehmen.¹¹ Auch die Raucherentwöhnung solltest du gezielt thematisieren. Ein vorübergehender Umstieg auf die E-Zigarette¹² kann dabei helfen, den Ausstieg schrittweise zu erleichtern.
Psychische Faktoren nicht unterschätzen
Nicht zu unterschätzen sind zudem psychische Faktoren wie emotionaler Stress¹³’¹⁴ und Depressionen, die sich direkt auf die Mundgesundheit auswirken können (Abb. 4).¹⁵ Achtsamkeitsmeditationen¹⁶’¹⁷ können helfen, Ängste zu reduzieren, ebenso kann körperliche Betätigung als Ausgleich empfohlen werden.¹⁸
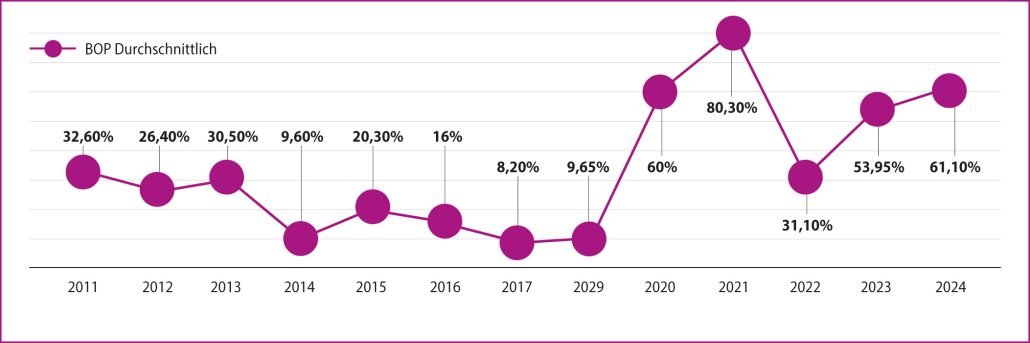
Stressbelastung zu einer deutlichen Verschlechterung kam (Abb. 4).
Hormonelle Veränderungen bei Frauen
Bei Frauen sind zudem hormonelle Veränderungen relevant: Schwankungen während des Zyklus, in der Schwangerschaft oder in den Wechseljahren beeinflussen die Entzündungsneigung. Dies ist auf Progesteron und Östrogen zurückzuführen, welche nachweislich die Immunantwort und den oralen Biofilm verändern.¹⁹’²⁰ Ein Mangel an Östrogen führt zudem zu einem erheblichen Verlust der Knochenstärke, wodurch das Osteoporoserisiko²¹ ansteigt – ein Aspekt, der direkt mit Ernährung und parodontaler Gesundheit verknüpft ist.
Strategie 3: Ernährung und Mängel hinterfragen
Eine mediterrane Kost mit viel Obst, Gemüse, Vollkornprodukten und ungesättigten Fettsäuren kann entzündungshemmend wirken, auch wenn hierzu noch weitere Studien erforderlich sind. Ergänzend können Mikronährstoffe eine unterstützende Rolle spielen.
Vitamin D, C, A, E, B²² sowie Omega-3-Fettsäuren²³ beeinflussen die Immunfunktion und Entzündungsregulation. Auch wenn sie keine kausale Therapie ersetzen, können sie insbesondere bei älteren oder gesundheitlich eingeschränkten Patientinnen und Patienten einen positiven Beitrag leisten.
Strategie 4: Adjuvantien gezielt einsetzen
Von zentraler Bedeutung ist der gezielte Einsatz lokaler Adjuvantien, von denen mittlerweile eine große Vielfalt auf dem Markt existiert.
PVP-Jod als Spülung
Stellvertretend seien lokal wirkende Ansätze wie PVP-Jod genannt. Dieses kannst du als Spülung oder als Kühlflüssigkeit bei der subgingivalen Anwendung von Ultraschall einsetzen und kannst die Sondierungstiefen und den klinischen Attachmentlevel der Patientinnen und Patienten leicht verbessern.²⁴
Lokal appliziertes Antibiotikum
Lokal appliziertes Antibiotikum kann parodontitisassoziierte Keime gezielt in tiefen oder schwer zugänglichen Taschen reduzieren²⁵ und die nichtchirurgische Therapie sinnvoll ergänzen.
Ozon als unterstützende Maßnahme
Auch die Anwendung von Ozon wird als unterstützende Maßnahme genutzt, da es antibakterielle und entzündungshemmende Eigenschaften besitzt und zur Reduktion der mikrobiellen Belastung beitragen kann.²⁶’²⁷
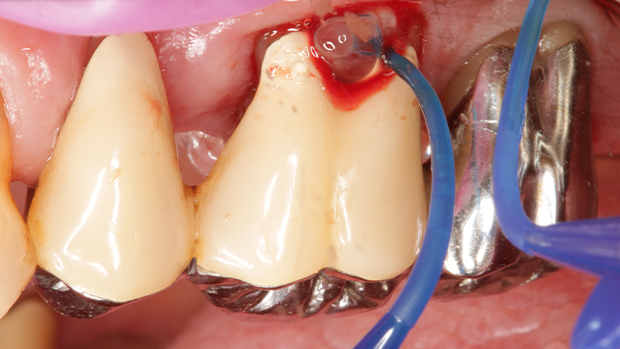
Pocket-X Gel für persistierende Taschen
Besonders bewährt hat sich das Pocket-X Gel, das direkt in persistierende Taschen appliziert werden kann. Das thermoreaktive Gel²⁸ geliert bei Körpertemperatur 37 Grad Celsius (Abb. 1) und bildet eine Barriere gegen die Wiederbesiedlung durch Bakterien. Dadurch verbleibt es stabil im Defekt und kann seine wundheilungsfördernde und antibakterielle Wirkung, basierend auf Hyaluron und Octenidin, optimal entfalten.²⁹ Dies macht es insbesondere für tiefe Taschen, Furkationen sowie schwer zugängliche Bereiche geeignet.
Neue Ansätze: PerioTrap
Neuere Produkte wie PerioTrap setzen darauf, parodontitisassoziierte Bakterien im Biofilm gezielt zu blockieren, ohne die gesamte Mundflora zu beeinträchtigen. Zwar liegen bislang keine groß angelegten klinischen Studien vor, dennoch stellt dies einen vielversprechenden Ansatz dar.
Palliativer Zahnerhalt als aktiver Behandlungsansatz mit klaren Zielen
Nicht der ideale Befund, sondern Funktion, Beschwerdefreiheit und Lebensqualität stehen im Vordergrund. Durch individuell angepasste Maßnahmen und kontinuierliche Betreuung lassen sich auch fortgeschrittene parodontale Situationen oft langfristig stabilisieren.
Du übernimmst dabei als Dentalhygienikerin, Zahnmedizinische Fachangestellte oder Praxismanagerin eine Schlüsselrolle als kontinuierliche Begleiterin zwischen fachlicher Betreuung, Prävention und dem Erhalt von Lebensqualität.
Literatur
- Nibali, L., et al. (2016): Tooth loss in molars with and without furcation involvement – a systematic review and meta-analysis. J Clin Periodontology.
- Graetz Ch. et al. (2019): Long-term survival and maintenance efforts of splinted teeth in periodontitis patients J Dent.
- Slot, D. E. (2020): Mechanical plaque removal of periodontal maintenance patients – A systematic review and network meta-analysis. Journal of Clinical Periodontology.
- Zhang, X., et al. (2016): Improving Children’s Competence as Decision Makers: Contrasting Effects of Collaborative Interaction and Direct Instruction. Sage Publications.
- Deinzer, R., et al. (2018): Sicherung des parodontalen Behandlungserfolgs – Stand der Forschung und Forschungsbedarf. Literatur-Trilogie, Teil 1: Die individuelle Mundhygiene. Zahnmed Forsch Vers (IDZ).
- Lorentz T. C. M. et al. (2009): Prospective study of complier individuals under periodontal maintenance therapy: analysis of clinical periodontal parameters, risk predictors and the progression of periodontitis. J Clin Periodontol.
- Ramseier, C. A., (2020): Impact of risk factor control interventions for smoking cessation and promotion of healthy lifestyles in patients with periodontitis: a systematic review. J Clin Periodontol.
- Sanz M, et al. (2020): Treatment of stage I-III periodontitis – The EFP S3 level clinical practice guideline.
- Jepsen, S. et al. (2020): The association of periodontal diseases with metabolic syndrome and obesity.
- Inchingolo F. et al. (2023): The Effects of Periodontal Treatment on Rheumatoid Arthritis and of Anti-Rheumatic Drugs on Periodontitis: A Systematic Review.
- https://newsroom.da-direkt.de/pressreleases/neujahrsvorsatz-gesundheit-deutsche-sind-vorsorgemuffel-3362403
- Tatullo M. et al. (2016): Crosstalk between oral and general health status in e-smokers.
- Hilgert et al. (2006): Stress, cortisol, and periodontitis in a population aged 50 years and over. J Dent Res.
- Hugo et al. (2006): Chronic stress, depression, and cortisol levels as risk indicators of elevated plaque and gingivitis levels in individuals aged 50 years and older. J Periodontol.
- Tikeshwari Gurav et al. (2024): Analyzing the Relationship Between Chronic Periodontitis and Psychological Stress in Elderly Patients: A Study Protocol. Cureus.
- Goyal, M., et al. (2013): Meditation programs for psychological stress and well-being: a systematic review and meta-analysis. JAMA Intern Med.
- Hoge, E.A. et al. (2013): Randomized controlled trial of mindfulness meditation for generalized anxiety disorder: effects on anxiety and stress reactivity. J Clin Psychiatry.
- Bretland R. J. et al. (2015): Reducing workplace burnout: the relative benefits of cardiovascular and resistance exercise. PeerJ.
- Muntaha Jawed S.T. et al. (2025): Understanding the Link Between Hormonal Changes and Gingival Health in Women: A Review.
- De Villiers T.J. (2024): Bone health and menopause: Osteoporosis prevention and treatment Best Practice & Research Clinical Endocrinology & Metabolism.
- Chunxiao L. et al. (2020): Effects of combined calcium and vitamin D supplementation on osteoporosis in postmenopausal women: a systematic review and meta-analysis of randomized controlled trials Food Funct.
- Mayank, H. et al. (2023): Serum levels of various vitamins in periodontal health and disease – a cross sectional study J Oral Biol Craniofac.
- Wölber J.P. et al. (2023): Dietary and Nutraceutical Interventions as an Adjunct to Non-Surgical Periodontal Therapy – A Systematic Review Nutrients.
- Svellenti, L. et al., (2024): Effects of Rinsing with Povidone-Iodine during Step II Periodontal Therapy: A Systematic Review and Meta-Analysis. J Clin Med.
- Herrera, D., et al. (2020): Adjunctive effect of locally delivered antimicrobials in periodontitis therapy. A systematic review and meta-analysis. J Clin Periodontol.
- Ramirez-Peña A.M. et al. (2022): Ozone in Patients with Periodontitis: A Clinical and Microbiological Study J Clin Med.
- Swarna Meenakshi P.; Rajasekar A. (2022): A review on ozone therapy in periodontitis Bioinformation.
- Chen Y, et al. (2021): An Overview on Thermosensitive Oral Gel Based on Poloxamer 407 Materials (Basel).
- Hirsch A. et al. (2022): A thermosensitive gel with an active hyaluronic acid ingredient that contains an octenidine preservation system as an adjunct to scaling and root planning: a randomized prospective clinical study Clin Oral Investig.
